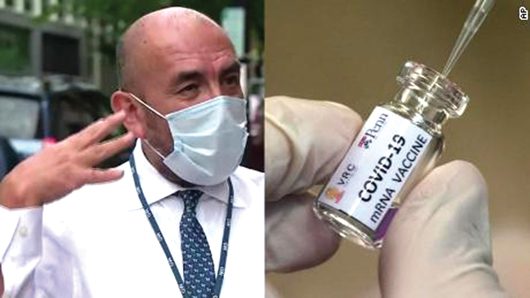
Médico peruano que radica en Washington recibió la primera dosis de la vacuna de Moderna contra el COVID-19 y dijo no haber sentido ninguna molestia.
La primera vacuna contra el coronavirus que está en la fase III del ensayo en seres humanos ha dado hasta ahora resultados positivos. La compañía de biotecnología Moderna ubicada en Cambridge, cerca de Boston, ya ha probado la vacuna en miles de voluntarios que se mostraron dispuestos a recibir la primera dosis. El reconocido médico peruano radicado en Washington, Elmer Huerta, es una de las 30,000 personas que participan en el ensayo clínico que dio como testimonio no haber “sentido ninguna molestia”.
El doctor Huerta confirmó haber asistido a aplicarse la primera dosis de la vacuna candidata contra el coronavirus de la empresa Moderna, en el hospital de la Universidad George Washington donde trabaja, señalando que a lo largo de cuatro semanas “voy a estar monitoreado por los doctores, hasta la siguiente dosis”.
El especialista en Salud pública dijo que es uno de los 30,000 voluntarios, de los cuales 15,000 recibirán la vacuna y el resto un placebo. “Aún no sé cuál de las dos dosis recibí”, anota.
“He tenido entrevistas con los doctores, me han hecho un examen completo, me han sacado ochos tubos de sangre y a las 8:53 de la mañana, en el brazo izquierdo, me pusieron la vacuna o el placebo”, dijo.
Este es el más ambicioso proyecto para hallar una vacuna contra el coronavirus.
Según los científicos de Moderna, para determinar la eficacia de la dosis, los voluntarios no sabrán si están recibiendo la vacuna o un placebo. Luego de dos inyecciones, serán monitoreados de cerca para ver cuál de los dos grupos desarrolla más infecciones al tiempo que prosigue con su rutina diaria, especialmente en regiones donde el virus ha resurgido.
Trabajan contrarreloj
Cientos de científicos y compañías farmacéuticas en varios países están trabajando contrarreloj y a toda máquina para desarrollar una vacuna.
Hay siete grupos de investigación que entraron en los ensayos de fase 3. Dos de ellos, las farmacéuticas Moderna y la compañía Pfizer, ya tienen grandes avances con humanos.
Moderna se ha concentrado en voluntarios en Estados Unidos, uno de los países más afectados por la enfermedad, mientras que Pfizer está realizando sus ensayos tanto en Estados Unidos como en Alemania, Argentina y Brasil, otro país duramente golpeado por el coronavirus.
La vacuna experimental de la Universidad de Oxford ya está en la fase final y busca analizar a miles de personas en países como Brasil, Sudáfrica y Reino Unido.
Las autoridades que lideran el desarrollo de la vacuna rusa anunciaron también que iniciarán, la próxima semana, pruebas clínicas con 40.000 personas, no sólo en Rusia sino en otros países.
Otro peruano de voluntario
El periodista peruano, Jesús Claros Muñoz, de 63 años, radicado en Argentina, fue uno de los 25,000 seleccionados para recibir la vacuna experimental de las compañías farmacéuticas Pfizer Inc. y BioNTech.
“Yo estaba como suplente y hace unas horas me llamaron para comunicarme mi inclusión en el grupo de seleccionados”, dijo Claros luego de que fue al Hospital Militar, sede del estudio. “No sentí miedo ser parte de un proyecto que podría beneficiar a millones de personas en todo el mundo”, anotó.
Su hija Flor Claros escribió en su página de Facebook: “Sentimientos encontrados, orgullosa de mi papi y a la vez temor por no saber qué efectos secundarios tendrá la vacuna, felicito su desprendimiento y su altruismo por el bien de los demás. Te amo papi”.
Vacuna sería gratuita para estadounidenses
La compañía de biotecnología Cambridge Biotech Moderna Inc. ya ha firmado un acuerdo para proporcionar más de 500 millones de dosis de su vacuna Covid-19 en Estados Unidos.
Funcionarios del gobierno estadounidenses señalan que planean pagar a Moderna (Nasdaq: MRNA) hasta $ 1,525 mil millones por 100 millones de dosis de su vacuna Covid-19, en caso de que tenga éxito. El fármaco se está probando actualmente en dos ensayos clínicos, incluida una prueba de fase 3 para 30.000 personas.
Estados Unidos también tiene la opción de comprar otros 400 millones de dosis.
El acuerdo valora cada dosis en $ 15.25, muy por debajo de los $ 32 a $ 37 que los ejecutivos de Moderna habían propuesto originalmente como estimación. La vacuna sería gratuita para los estadounidenses, según el Departamento de Salud y Servicios Humanos.
Pfizer (NYSE: PFE) acordó vender su candidata a vacuna a los EE. UU. A 20 dólares por dosis, mientras que Johnson & Johnson (NYSE: JNJ) ha estimado que una dosis de su medicamento podría costar 10 dólares.
Este es el segundo acuerdo importante de compra de vacunas que Moderna ha revelado. Ha recibido alrededor de $ 400 millones en depósitos de vacunas de varios países, incluido el gobierno canadiense. Ni el gobierno canadiense ni Moderna indicaron cuántas dosis se incluyeron en el pedido y qué precio se estaba pagando.
La vacuna de Moderna se administra en dos dosis con 30 días de diferencia. Los ejecutivos de la compañía han dicho anteriormente que la biotecnología tiene suficiente capacidad de fabricación para servir a toda la población de Estados Unidos.
No está claro en este momento cuándo Moderna podría comenzar a comercializar su vacuna, si pasa las pruebas en humanos. Moderna y otros fabricantes de medicamentos han expresado su interés en llevar sus vacunas al mercado temprano a través de la autorización de uso de emergencia de la FDA. Esa herramienta reguladora nunca se ha aplicado a una vacuna completamente nueva.
Prueban eficacia
de la vacuna
En los ensayos de fase 3, los investigadores prueban la eficacia de la vacuna, mientras monitorean las reacciones adversas en cientos de miles de voluntarios. Luego, la FDA aprueba la vacuna si los ensayos demuestran que es segura y eficaz, y los beneficios de la vacuna superan sus riesgos, según los Centros para el Control y la Prevención de Enfermedades (CDC).
Los ensayos de fase 3 ya han comenzado en Brasil y se inscribirán hasta 5.000 voluntarios. Se espera que otro ensayo de fase 3 inscriba a otras 10.500 personas en el Reino Unido y 30.000 en los EE. UU., Según la página web del ensayo de la vacuna de Oxford y The New York Times. El equipo de Oxford también ha expresado interés en realizar estudios de desafío en humanos, lo que significa que infectarían deliberadamente a voluntarios de bajo riesgo con el virus, ya sea junto con los ensayos de fase 3 o después de que estén completos, según The Guardian.
El Departamento de Salud y Servicios Humanos de EE. UU. (HHS) anunció que cedería hasta $ 1,2 mil millones a AstraZeneca para acelerar el proceso de desarrollo de la vacuna y ayudar a la empresa a fabricar al menos 300 millones de dosis de la vacuna, si resulta segura y eficaz. ya en octubre de 2020, según un comunicado. Esto es parte de la Operación Warp Speed de la administración Trump, una iniciativa que tiene como objetivo entregar 300 millones de dosis de una vacuna segura y efectiva para enero de 2021, según el HHS.
Las vacunas de ARNm han demostrado ser «una alternativa prometedora» a las vacunas tradicionales.







